以下表格统计自“国家药监局网站自2023年起发布至今的飞检通告”↘
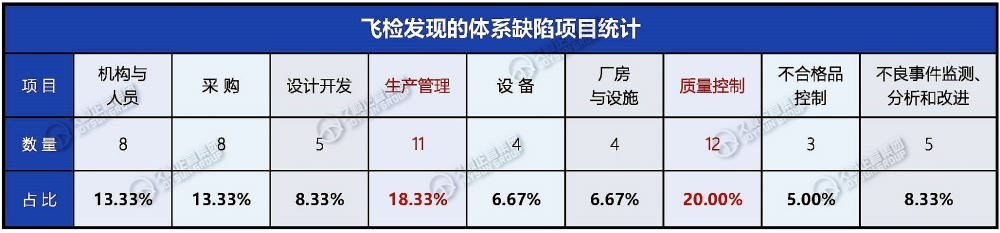
质量控制缺陷项目共出现12次,占比20%,为发生频率最高的缺陷,成为重灾区。生产管理次之,共出现11次,占比18%。其后为:机构与人员、采购.......
国家药品监督管理局组织检查组对江苏X生物医药技术股份有限公司、新疆X生物科技有限公司进行飞行检查,发现企业质量管理体系存在严重缺陷。
一、江苏X生物医药技术股份有限公司
(一)采购方面。抽查磁珠原材料的检验操作规程、检验记录单、原材料合格报告单,缺少磁珠直径和固含量的质量检测数据,企业与磁珠原材料供应商的质量及售后服务协议未规定对磁珠的质量要求,不符合《医疗器械生产质量管理规范》(以下简称《规范》)中企业应当对采购物品进行检验或者验证,确保满足生产要求的要求。
(二)质量控制方面。阳性质控品和阴性质控品原材料检测项目不完整,未进行紫外分光光度计扫描记录核酸吸收峰,与产品技术要求不一致,不符合《规范》中企业应当根据强制性标准以及经注册或者备案的产品技术要求制定产品的检验规程,并出具相应的检验报告或者证书的要求。
企业现场未提供阳性、阴性质控品所用细胞的细胞库档案资料和细胞操作日志,不符合《医疗器械生产质量管理规范附录体外诊断试剂》(以下简称《附录》)中应当建立细胞库档案资料和细胞操作日志的要求。
二、新疆X生物科技有限公司
(一)质量控制方面。企业免疫球蛋白A测定试剂盒(免疫比浊法)成品检验规程中规定的检测项目少于产品技术要求中载明的检测项目,且未进行风险评估,不符合《规范》中企业应当根据强制性标准以及经注册或者备案的产品技术要求制定产品的检验规程,并出具相应的检验报告或者证书的要求。
抽查免疫球蛋白A测定试剂盒(免疫比浊法)成品检验数据记录,公司不能提供“线性范围”项目中的线性样本来源的信息,不符合《规范》中每批(台)产品均应当有检验记录,并满足可追溯的要求。
(二)不良事件监测、分析和改进方面。抽查企业2023年度管理评审报告,该报告中管理评审汇报材料的制作日期,早于材料内汇报的内审工作开展日期,存在时间逻辑错误,不符合《规范》中企业应当定期开展管理评审,对质量管理体系进行评价和审核,以确保其持续的适宜性、充分性和有效性的要求。
上述2家企业质量管理体系存在严重缺陷,不符合《规范》相关规定。企业已对上述质量管理体系存在缺陷予以确认。
相关属地省级药品监督管理部门应当按照《医疗器械监督管理条例》第七十二条规定,依法采取责令暂停生产的控制措施;对涉嫌违反《医疗器械监督管理条例》及相关规定的,应当依法处理;责令企业评估产品安全风险,对有可能导致安全隐患的,按照《医疗器械召回管理办法》规定召回相关产品。
企业完成全部缺陷项目整改后,经属地省级药品监督管理部门复查合格方可恢复生产。
国家药品监督管理局组织检查组对贵州XXX有限公司、湖北X医疗器械有限公司进行飞行检查,发现两家企业的质量管理体系存在严重缺陷。
一、贵州XXX有限公司
(一)设备方面。企业某生产车间纯化水储存罐上方有开孔,储存罐内部直接和大气连通,无防护措施,不能有效防止污染,不符合《医疗器械生产质量管理规范附录无菌医疗器械》中应当确定所需要的工艺用水,配备相应的制水设备,并有防止污染措施的要求。
(二)生产管理方面。抽查企业某批次一次性使用吸引连接管生产记录,记录中未包含原材料色母和环己酮批次及用量信息;现场发现无标识的色母料(太青蓝),企业未能提供该物料采购、出入库和领用记录;聚氯乙烯(PVC)回用料情况不可追溯;企业某生产车间中的合格品区存放有无标识的一次性使用吸引连接管半成品,其旁无标识区域混放有无标识的生产过程不合格品,企业未能提供上述半成品和不合格品的数量和批次信息,不符合《医疗器械生产质量管理规范》(以下简称《规范》)中应当在生产过程中标识产品的检验状态,防止不合格中间产品流向下道工序的要求。
(三)不合格品控制方面。企业受控文件规定,对存在破损、尺寸不合格等情况的连接头、连接管等原材料,经过评审合格,可经破碎后投入回用,但抽查企业某批次一次性使用吸引连接管不合格品处置记录,显示企业将上述相关不合格原材料直接经过破碎后回用,未按照企业受控文件的规定对不合格品进行标识、记录、隔离、评审,不符合《规范》中应当对不合格品进行标识、记录、隔离、评审,根据评审结果,对不合格品采取相应的处置措施的要求。
二、湖北X医疗器械有限公司
(一)设备方面。企业注塑车间某注塑设备工作温度值超出该设备工艺卡规定的工作温度范围,企业未采取相应处置措施,不符合《规范》中企业应当配备与所生产产品和规模相匹配的生产设备、工艺装备等,并确保有效运行的要求。
(二)生产管理方面。现场检查时,企业未能提供如特殊工序使用的某封口机、关键工序使用的某注塑机等部分生产设备的验证记录,不符合《规范》中应当编制生产工艺规程、作业指导书等,明确关键工序和特殊过程的要求。
企业未记录粉碎房内粉碎机设备使用、破碎料总量,不能追溯回料使用次数;抽查企业某批次产品环氧乙烷灭菌记录,显示加药重量为13.5 Kg,但经现场了解,实际操作中,企业操作人员在加入整罐环氧乙烷气体后(约13.5 Kg),通过观察压力表数值确认是否达到灭菌浓度,如压力不足再加入另一罐气体至压力到达相应浓度,上述实际操作加药量与灭菌批记录中显示加药量不一致,不符合《规范》中每批产品均应当有生产记录,并满足可追溯的要求。
企业PP料粉碎房外堆放有无标识的待用物料;ABS料粉碎房内搅拌机内正在搅拌的粒料、混合料无标识,现场查见的物料储存箱上标识为PE高密度聚乙烯;企业声称过滤膜原材料由员工个人保管,检查时企业仅展示提供了无标识的一袋未封口包装的过滤膜,上述物料状态不可追溯,不符合《规范》中应当在生产过程中标识产品的检验状态,防止不合格中间产品流向下道工序的要求。
(三)质量控制方面。抽查企业某批次产品成品检验报告,报告中记录有环氧乙烷残留检测、沉降菌监测日期以及检测人和复核人信息,但进一步检查企业发现上述检测和复核人员在记录显示日期当天并不在岗;现场查见企业配制的胰酪大豆蛋白胨琼脂平皿数量与配制记录中记录的数量不一致,企业未能提供相关领用台账,不符合《规范》中每批产品均应当有检验记录,并满足可追溯的要求。
上述2家企业质量管理体系存在严重缺陷,不符合《医疗器械生产质量管理规范》《医疗器械生产质量管理规范附录无菌医疗器械》等法规相关要求,企业已对上述存在问题予以确认。
属地省级药品监督管理部门应当按照《医疗器械监督管理条例》第七十二条规定,依法采取责令暂停生产的控制措施,必要时开展监督抽检;对涉嫌违反《医疗器械监督管理条例》及相关规定的,依法处理;责令企业评估产品安全风险,对有可能导致安全隐患的,按照《医疗器械召回管理办法》规定召回相关产品;企业完成全部缺陷项目整改后,经属地省级药品监督管理部门复查合格方可恢复生产。
来源:国家药监局官网
声明:文章为转载,其版权归原作者所有。转载仅用于分享,若涉及文章版权等问题,联系我方删除!
>> 如需:国内质量管理体系\欧盟ISO13485体系\美国QSR820体系\MDSAP等培训、咨询和注册资料辅导服务,久顺企管定是您的上佳选择!
久顺始创于1996年,近30年全球合规技术专家,西班牙\荷兰\英国\美国\中国均设公司,专注无菌\非无菌\植入\有源\体外诊断等医疗器械领域,具备丰厚的质量体系、临床试验、产品注册咨询管理和技术服务经验,护航产品全球畅行无阻。





