11月13日,国家药监局网站同一天内连发6项医疗器械厂商主动召回信息,其中涉及:美敦力、雅培、奥林巴斯等知名械企,具体内容如下:
日本世诺临床诊断制品株式会社Shino-Test Corporation对高密度脂蛋白胆固醇测定试剂盒(直接法)主动召回
日立诊断产品(上海)有限公司报告,由于产品日文标识标签修订原因,生产商日本世诺临床诊断制品株式会社Shino-Test Corporation对其生产的高密度脂蛋白胆固醇测定试剂盒(直接法)QUICKAUTO NEO HDL-C(国械注进20152400907)主动召回。召回级别为三级召回。
雅培心血管Abbott Vascular对PTCA手术配件主动召回
雅培医疗器械贸易(上海)有限公司报告,由于产品泄漏可能性增加的原因,生产商雅培心血管Abbott Vascular对其生产的PTCA手术配件Accessories for PTCA(国械注进20173036805)主动召回。召回级别为二级召回。
史密斯医疗ASD有限公司Smiths Medical ASD, INC. 对一次性使用高流量温液管路及附件主动召回
史密斯医疗器械(上海)有限公司报告,由于用户无法正确安装,生产商史密斯医疗ASD有限公司Smiths Medical ASD, INC.对其生产的一次性使用高流量温液管路及附件Normothermic I.V. Fluid Administration Set and Accessories(国械注进20163141672)主动召回。召回级别为二级召回。
美敦力公司Medtronic Inc.对动静脉插管主动召回
美敦力(上海)管理有限公司报告,由于产品错误组装,生产商美敦力公司Medtronic Inc.对其生产的动静脉插管Arterial and Venous Cannula(国械注进20173100243)主动召回。召回级别为二级召回。
奥林巴斯医疗株式会社对电子上消化道内窥镜等产品主动召回
奥林巴斯贸易(上海)有限公司报告,由于产品被错误地发送给客户并使用的原因,生产商奥林巴斯医疗株式会社对其生产的电子上消化道内窥镜(国械注进20172061450)、电子胆道内窥镜(国械注进20232060312)、内窥镜摄像装置(国械注进20192060469)主动召回。召回级别为三级召回。
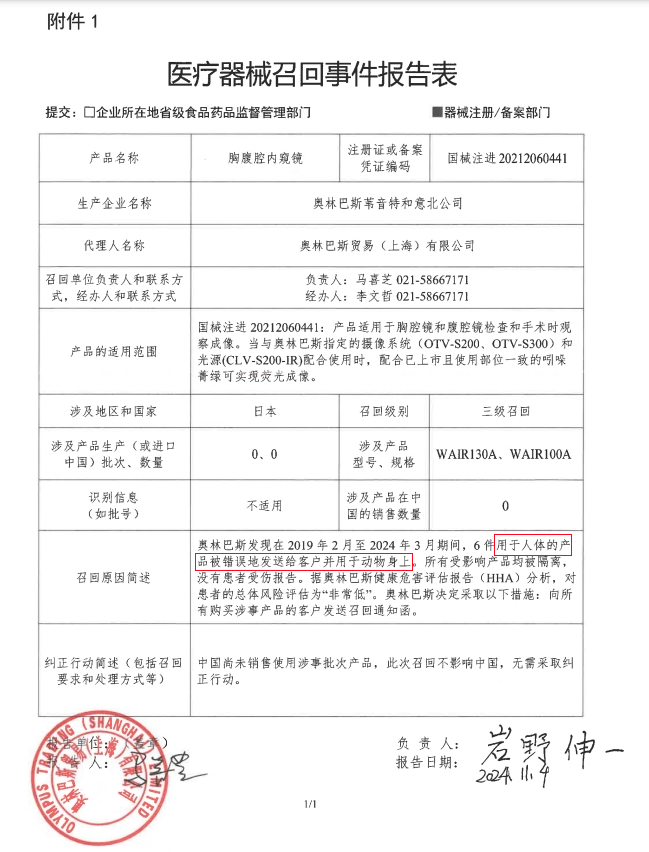
奥林巴斯苇音特和意北公司对胸腹腔内窥镜主动召回
奥林巴斯贸易(上海)有限公司报告,由于产品被错误地发送给客户并使用的原因,生产商奥林巴斯苇音特和意北公司对其生产的胸腹腔内窥镜(国械注进20212060441)主动召回。召回级别为三级召回。
召回原因:2019年2月至2024年3月期间,6件用于人体的产品被错误地发送给客户并用于动物身上。
来源:国家药监局
声明:文章为转载,其版权归原作者所有。转载仅用于分享,若涉及文章版权等问题,联系我方删除!



