一、IVDR过渡期延长修正案
2024年7月9日,欧盟官方期刊正式发表IVDR过渡期延长修正案并即刻生效。本次法规修订旨在为患者和医疗服务提供者提高体外诊断可用性,给予企业更多时间以过渡到欧盟IVD新规则,对制造商提出新义务(即在某些医疗设备的供应中断时通知国家当局和卫生部门),并允许逐步推出欧洲医疗器械数据库。
二、Others产品的IVDR延期规定
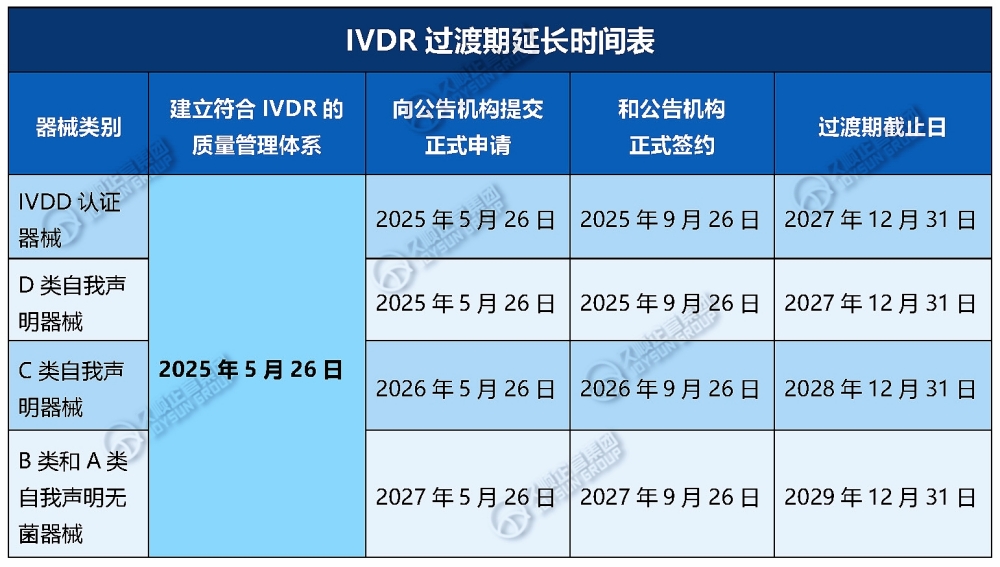
1.首次延期:IVDD下属于Others而在IVDR属于B/C/D类, 获得IVDD CE注册后,根据延期政策IVD遗留器械以下过渡期截止日:
| 器械分类 | 过渡期 |
| D类自我声明器械 | 2025年5月26日 |
| C类自我声明器械 | 2026年5月26日 |
| B类和A类自我声明器械 | 2027年5月26日 |
2.再次延期:IVDD下属于Others而在IVDR属于B/C/D类, 获得IVDD CE注册后,取得NB机构的延期信函,根据延期政策可持续使用直至IVD遗留器械以下过渡期截止日:
| 器械分类 | 延期信函过渡期 |
| D类自我声明器械 | 2027年12月31日 |
| C类自我声明器械 | 2028年12月31日 |
| B类和A类自我声明器械 | 2029年12月31日 |
需满足以下条件:a.应继续符合指令98/79/EC;b.器械设计和预期用途无重大变化;c.不对患者、使用者或他人健康或安全,或保护公众健康等造成不可接受的风险;d.2025年5月26日之前,制造商已升级质量管理体系,已符合EN ISO 13485和IVDR适用条款要求;e.制造商已向公告机构提交正式申请或签署认证合同对产品进行合格评定,不迟于以下时间:
| 器械分类 | 签约时间 |
| D类自我声明器械 | 2025年9月26日 |
| C类自我声明器械 | 2026年9月26日 |
| B类和A类自我声明器械 | 2027年9月26日 |
三、时间不多!给制造商的重要合规提示
1.距离建立符合IVDR的质量体系截止日,仅剩6个月,建议尽快取得ISO13485体系证书!
2.D类器械CE办证时间至少需要24个月,目前时间已不足,D类产品尽快启动办证工作!
3.C类器械CE办证平均周期为18个月,建议立即启动C类办证!
4.部分公告机构IVDR技术文档作为签约的前提条件。因此,制造商应准备的IVDR技术文档是当务之急!
四、久顺集团技术服务,IVDR专业服务
1. 久顺提供体系建立和体系升级服务,目前已为几十家IVD企业完成体系辅导工作,包含IVD上市公司、集团公司和新的IVD企业。
2. D类器械CE办证的重点是临床试验,久顺与欧洲多个实验室合作,可为企业提供欧洲临床试验服务,小批量临床研究,可用性研究,也可为企业提供IVDR技术文档编写、ISO13485体系建立和升级。
3. C类器械CE办证不少产品需要做欧洲临床试验,久顺与欧洲多个实验室合作,可为企业提供欧洲临床试验服务,小批量临床研究,可用性研究,也可为企业提供IVDR技术文档编写、ISO13485体系建立和升级。如产品成熟,有国内或国外临床数据,久顺可提供临床报告编写服务。
4. B类,C类和D类产品,想快速签约机构,可以选择与久顺合作IVDR技术文档编写,也可提供IVDR技术文档合规服务。
久顺拥有IVDR B类自测、B类和C类的成功取证经验,高效合规的IVDR专业服务,久顺一直是IVD企业优先的选择、忠实的朋友、成功的伙伴。
久顺是IVD企业合规路上的加速引擎!始创于1996年,近30年全球合规技术专家,近20年资深欧代,在西班牙\荷兰\英国\美国\中国均设公司。
久顺近30年始终如一为医疗企业提供优质的服务,选择久顺,是选择了一家长期稳定的合作伙伴,久顺愿与您携手同行!








 沪公网安备 31011502005499
沪公网安备 31011502005499